资料与方法
一、对象
二、仪器与方法
三、统计学分析
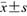 表示,CHMCF与PHMF组间差异比较采用t检验,受孕方式、阴道流血、孕6~10周孕囊旁异常回声、黄素化囊肿和滋养细胞肿瘤(gestational trophoblastic neoplasia, GTN)例数为计数资料,采用例数(%)表示,采用χ2检验比较组间差异。P<0.05为差异具有统计学意义。
表示,CHMCF与PHMF组间差异比较采用t检验,受孕方式、阴道流血、孕6~10周孕囊旁异常回声、黄素化囊肿和滋养细胞肿瘤(gestational trophoblastic neoplasia, GTN)例数为计数资料,采用例数(%)表示,采用χ2检验比较组间差异。P<0.05为差异具有统计学意义。结果
一、CHMCF临床、超声表现及预后
表1 CHMCF病例的临床表现、超声特征及妊娠结局 |
| 病例编号 | 年龄(岁) | 孕次(次) | 受孕方式 | 血β-hCG值(mIU/ml) | 阴道出血 | 超声诊断结果 | 首次诊断时的怀孕天数(d) | 病变部位最大径(cm) | 病变部位与胎盘关系 | 胎儿有无异常 | 黄素化囊肿 | 孕6~10周超声表现 | 妊娠结局 | 免疫组化结果 | 染色体检测结果 | 滋养细胞肿瘤 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 38 | 2 | IVF | >200 000 | 有 | CHMCF | 63 | 8.6 | 无明显关系 | 无 | 无 | 双孕囊 | 38周剖宫产一活女婴 | p57Kip2(-) | 46,XX | 无 |
| 2 | 35 | 2 | IVF | >200 000 | 有 | PHMF | 83 | 9.8 | 与胎盘边缘紧贴 | 无 | 无 | 孕囊旁无回声,内见絮状稍强回声 | 引产 | p57Kip2(-) | 未查 | 无 |
| 3 | 27 | 1 | IVF | >200 000 | 有 | CHMCF | 85 | 5.9 | 与胎盘边缘紧贴 | 无 | 无 | 孕囊旁无回声,内见絮状稍强回声 | 引产 | p57Kip2(-) | 未查 | 无 |
| 4 | 27 | 1 | 自然 | >200 000 | 有 | CHMCF | 67 | 9.7 | 无明显关系 | 胎儿较停经时间小5 d | 无 | 孕囊旁无回声 | 引产 | p57Kip2(-) | 未查 | 无 |
| 5 | 31 | 2 | 自然 | 44 323.8 | 有 | 胎盘或胎膜发育异常 | 135 | 10.5 | 距胎盘1.2 cm | 无 | 无 | 孕囊旁杂乱回声 | 剖宫取胎 | p57Kip2(-) | 未查 | 无 |
| 6 | 38 | 6 | 自然 | >200 000 | 有 | CHMCF | 103 | 13.2 | 与胎盘无明显关系 | 胎儿较停经时间小7 d | 有 | 孕囊旁杂乱回声 | 引产 | p57Kip2(-) | 未查 | 无 |
| 7 | 32 | 4 | 自然 | >200 000 | 有 | PHMF | 90 | 8.0 | 与胎盘无明显关系 | 无 | 有 | 孕囊旁无回声 | 引产 | p57Kip2(-) | 未查 | 无 |
注:CHMCF为双胎之一完全性葡萄胎,PHMF为部分性葡萄胎合并胎儿存活,IVF为体外受精,β-hCG为β人绒毛膜促性腺激素 |
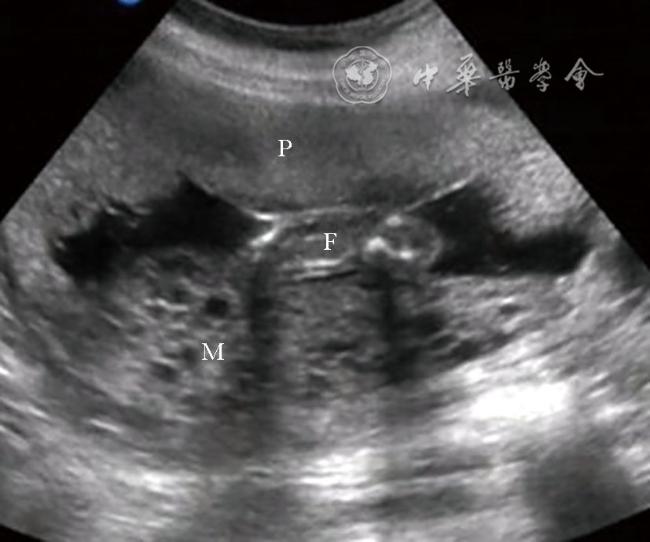
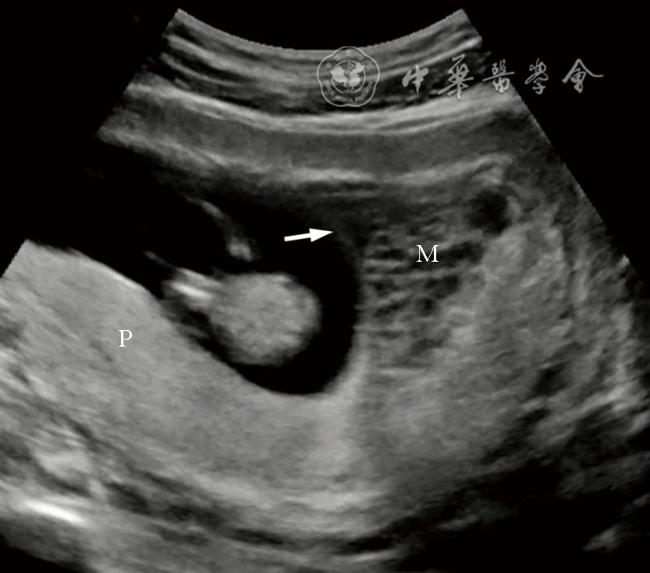
图1 病例1,孕妇38岁,体外受精-胚胎移植术后,移植2枚胚胎,孕22周超声检查显示胎盘(P)位于子宫前壁,葡萄状水泡回声(M)位于子宫后壁,与胎盘分界清楚注:F为胎儿 |
二、PHMF临床、超声表现及预后
表2 PHMF病例的临床表现、超声特征及妊娠结局 |
| 病例编号 | 年龄(岁) | 孕次(次) | 受孕方式 | 血β-hCG值(mIU/ml) | 阴道出血 | 超声诊断结果 | 首次诊断时的怀孕天数(d) | 病变部位最大径(cm) | 病变部位与胎盘关系 | 胎儿有无异常 | 黄素化囊肿 | 孕6~10周超声表现 | 妊娠结局 | 免疫组化结果 | 染色体检测结果 | 滋养细胞肿瘤 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 8 | 27 | 2 | 自然 | 170 827 | 无 | PHMF | 87 | 5.6 | 与胎盘紧贴,分界不清 | 无 | 无 | 无特殊 | 引产 | p57Kip2(+) | 未查 | 无 |
| 9 | 38 | 2 | 自然 | 87 604.3 | 无 | PHMF | 90 | 未测量 | 胎盘内 | 无 | 无 | 无特殊 | 引产 | p57Kip2(+) | 未查 | 无 |
| 10 | 29 | 1 | 自然 | >200 000 | 无 | PHMF | 84 | 未测量 | 胎盘内 | 无 | 无 | 无特殊 | 引产 | p57Kip2(+) | 未查 | 无 |
| 11 | 27 | 1 | 自然 | >200 000 | 有 | PHMF | 84 | 未测量 | 胎盘内 | 胎儿较停经时间小4 d | 无 | 无特殊 | 引产 | p57Kip2(+) | 未查 | 无 |
| 12 | 32 | 3 | 自然 | 31 836.6 | 无 | PHMF | 79 | 未测量 | 胎盘内 | 无 | 无 | 无特殊 | 引产 | p57Kip2(+) | 未查 | 无 |
| 13 | 36 | 3 | 自然 | >200 000 | 有 | PHMF | 133 | 7.2 | 与胎盘紧贴,分界不清 | 无 | 无特殊 | 剖宫取胎 | p57Kip2(+) | 未查 | 无 | |
| 14 | 36 | 5 | IVF | >200 000 | 无 | PHMF | 88 | 未测量 | 胎盘内 | 无 | 无 | 无特殊 | 引产 | p57Kip2(+) | 未查 | 无 |
| 15 | 29 | 2 | 自然 | 149 071 | 有 | PHMF | 112 | 10.5 | 胎盘内 | 脐膨出 | 无 | 无特殊 | 引产 | p57Kip2(+) | 未查 | 无 |
| 16 | 23 | 2 | 自然 | >200 000 | 无 | PHMF | 131 | 16.2 | 与胎盘紧贴,分界不清 | 无 | 无 | 孕囊旁无回声 | 剖宫取胎 | p57Kip2(+) | 未查 | 有 |
注:PHMF为部分性葡萄胎合并胎儿存活,IVF为体外受精,β-hCG为β人绒毛膜促性腺激素 |
三、CHMCF和PHMF的临床表现、超声特征的比较
表3 CHMCF和PHMF的临床表现、超声特征的比较 |
| 项目 | CHMCF(n=7) | PHMF(n=9) | 统计值 | P值 |
|---|---|---|---|---|
年龄(岁,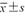 ) ) | 32.6±4.6 | 30.8±5.0 | t=-0.737 | 0.473 |
孕次(次,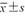 ) ) | 2.6±1.8 | 2.3±1.2 | t=-0.299 | 0.771 |
| IVF-ET例数[例(%)] | 3(42.9) | 1(11.1) | χ2=2.116 | 0.262 |
| 阴道出血[例(%)] | 7(100) | 3(33.3) | χ2=7.467 | 0.011 |
首次诊断怀孕天数(d,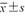 ) ) | 89.4±24.2 | 98.7±21.0 | t=-0.844 | 0.415 |
| 孕6~10周孕囊旁异常回声[例(%)] | 7(100) | 1(11.1) | χ2=12.444 | 0.001 |
| 黄素化囊肿[例(%)] | 2(28.5) | 0(0) | χ2=2.939 | 0.175 |
| GTN[例(%)] | 0(0) | 1(11.1) | χ2=0.830 | 1.000 |
注:CHMCF为双胎儿之一完全性葡萄胎,PHMF为部分性葡萄胎合并胎儿存活,IVF-ET为体外受精-胚胎移植,GTN为滋养细胞肿瘤 |