资料与方法
一、对象
二、仪器与方法
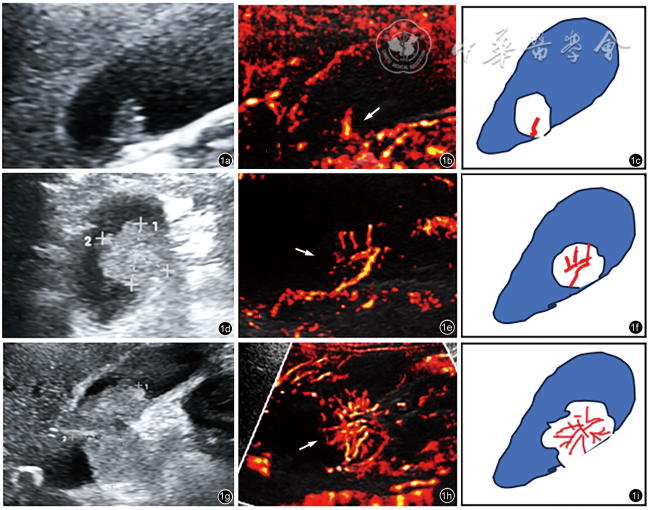
图1 超分辨超声显示胆囊息肉样病变血流模式图(箭头所示为病变处)。图a、d、g为常规超声显示胆囊息肉样病变;图b、e、h为超分辨超声下胆囊息肉样病变血流形态图;图c、f、i为胆囊息肉样病变不同血流形态模式示意图;图a~c为Ⅰ级血流图像;图d~f为Ⅱ级血流图像;图g~i为Ⅲ级血流图像 |
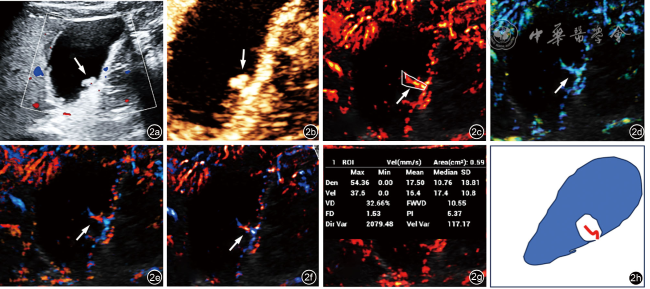
图2 胆囊息肉样病变超声多模态检查(箭头所示为病变处)。图a为常规超声显示胆囊后壁息肉样病变;图b为超声造影显示该病灶静脉期持续增强;图c为超分辨超声显示胆囊息肉内条棒状血流(血管密度图);图d为超分辨超声显示胆囊息肉内条棒状血流(血流速度图);图e为超分辨超声显示胆囊息肉内条棒状血流(血管速度方向图);图f为超分辨超声显示胆囊息肉内条棒状血流(血管密度方向图);图g为超分辨超声对胆囊息肉内血流进行定量分析,获得血流速度(VEL)、血管密度(VD)、血流容积(FWVD)、分形维数(FD)、灌注指数(PI)、方向方差(Dir Var)及速度方差(Ver Var)各定量参数值;图h为示意图显示超分辨超声胆囊肿块血流形态呈条棒状,为Ⅰ型血流模式 |
三、统计学分析
结果
一、患者一般特征
二、胆囊肿瘤性息肉与非肿瘤性息肉常规超声及超声造影特征比较
表1 胆囊肿瘤性息肉与非肿瘤性息肉各模态超声特征比较 |
| 超声特征 | 非肿瘤性息肉(n=40) | 肿瘤性息肉(n=46) | 统计值 | P值 |
|---|---|---|---|---|
| 常规超声 | ||||
| 病变大小(mm) | 14(10,18) | 24(16,35) | Z=-4.410 | <0.001 |
| 数量 | χ2=8.167 | 0.004 | ||
| 单个 | 24(60.00) | 40(86.95) | ||
| 多个 | 16(40.00) | 6(13.05) | ||
| 位置 | χ2=1.275 | 0.529 | ||
| 底部 | 14(35.00) | 21(45.65) | ||
| 体部 | 24(60.00) | 22(47.83) | ||
| 颈部 | 2(5.00) | 3(6.52) | ||
| 形状 | χ2=2.981 | 0.225 | ||
| 长形 | 13(32.50) | 11(23.91) | ||
| 圆形 | 10(25.00) | 7(15.22) | ||
| 椭圆形 | 17(42.50) | 28(60.87) | ||
| 回声 | χ2=0.130 | 0.719 | ||
| 均匀 | 25(62.50) | 27(58.70) | ||
| 不均匀 | 15(37.50) | 19(41.30) | ||
| 基底 | χ2=7.523 | 0.006 | ||
| 窄基底(有蒂) | 20(50.00) | 35(76.09) | ||
| 宽基底(无蒂/广基) | 20(50.00) | 11(23.91) | ||
| 胆囊壁 | χ2=3.958 | 0.047 | ||
| 连续 | 30(75.00) | 25(54.35) | ||
| 不连续 | 10(25.00) | 21(45.65) | ||
| 表面轮廓 | χ2=0.000 | 1.000 | ||
| 规则 | 23(57.50) | 20(43.48) | ||
| 不规则 | 17(42.50) | 26(56.52) | ||
| 血流信号 | χ2=16.48 | 0.001 | ||
| 存在 | 17(42.50) | 35(76.09) | ||
| 不存在 | 23(57.50) | 11(23.91) | ||
| 胆囊结石或胆泥 | χ2=0.310 | 0.578 | ||
| 存在 | 6(15.00) | 9(19.57) | ||
| 不存在 | 34(85.00) | 37(80.43) | ||
| 超声造影 | ||||
| 动脉期增强情况 | χ2=1.390 | 0.238 | ||
| 高增强 | 32(80.00) | 41(89.13) | ||
| 等/低增强 | 8(20.00) | 5(10.87) | ||
| 静脉期廓清情况 | χ2=13.274 | <0.001 | ||
| 早廓清 | 8(20.00) | 27(58.70) | ||
| 同步/不廓清 | 32(80.00) | 19(41.30) | ||
| 超分辨超声 | ||||
| 血流形态 | χ2=38.894 | <0.001 | ||
| Ⅰ级血管模式 | 32(80.00) | 6(13.04) | ||
| Ⅱ级血管模式 | 4(10.00) | 20(43.48) | ||
| Ⅲ级血管模式 | 4(10.00) | 20(43.48) | ||
| 血流定量参数 | ||||
| 血流速度(mm/s) | 17.09±0.75 | 21.43±0.68 | t=-4.721 | <0.001 |
| 分形维数 | 1.46(1.32,1.56) | 1.61(1.55,1.68) | Z=-5.142 | <0.001 |
| 血管密度 | 33.57±15.95 | 45.08±13.56 | t=-3.616 | 0.001 |
| 血流容积 | 4.66(2.54,7.98) | 8.96(6.36,12.60) | Z=-4.126 | <0.001 |
| 灌注指数 | 4.98(2.94,9.15) | 9.42(7.02,13.22) | Z=-3.991 | <0.001 |
| 方向方差 | 1985.30(1535.44,2304.48) | 2047.45(1808.58,2262.04) | Z=-0.857 | 0.391 |
| 速度方差 | 157.58(121.90,212.32) | 181.85(138.08,212.75) | Z=0.391 | 0.299 |
注:表格中符合正态分布的计量资料以 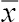 |
三、胆囊肿瘤性息肉与非肿瘤性息肉超分辨超声参数比较
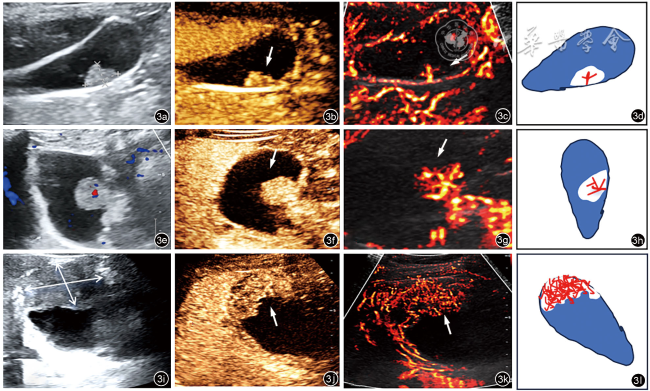
图3 胆囊息肉样病变超声多模态图像及示意图(箭头所示为病变处)。图a为常规超声显示胆囊后壁胆固醇性息肉,最大径>10 mm;图b为超声造影显示该病灶90 s静脉期持续增强;图c为超分辨超声显示病灶内为条棒状血流;图d为示意图显示2级分支,为Ⅰ型血流模式。图e为常规超声显示胆囊后壁胆囊腺瘤,大小18 mm×16 mm,内似见点状血流;图f为超声造影显示该病灶60 s静脉期持续增强;图g为超分辨超声显示病灶内为分支状血流;图h为示意图显示3级分支,为Ⅱ型血流模式。图i为常规超声显示胆囊底部占位,大小45 mm×33 mm;图j为超声造影显示该病灶45 s静脉期早廓清;图k为超分辨超声显示胆囊病灶内丰富杂乱血流;图l为示意图显示病灶内为丰富杂乱血流,为Ⅲ型血流模式 |
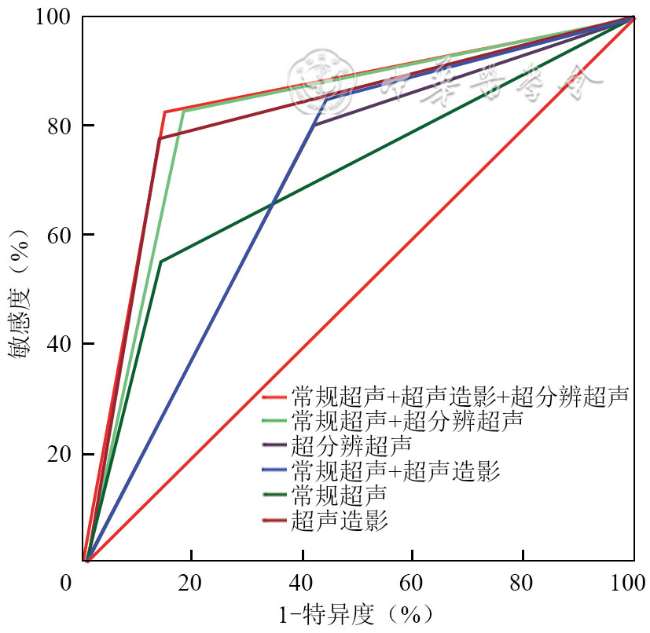
四、各参数诊断胆囊肿瘤性息肉的ROC曲线分析
表2 常规超声及超声造影各特征鉴别胆囊肿瘤性息肉与非肿瘤性息肉的诊断效能比较 |
| 诊断特征 | AUC(95%CI) | 敏感度(%) | 特异度(%) | 阳性预测值(%) | 阴性预测值(%) | 准确性(%) |
|---|---|---|---|---|---|---|
| 常规超声特征 | ||||||
| 息肉最大径≥14.5 mm | 0.71(0.60~0.82) | 69.00 | 78.60 | 87.00 | 55.00 | 72.09 |
| 单发 | 0.64(0.51~0.75) | 62.50 | 72.70 | 87.00 | 40.00 | 65.11 |
| 测及血流 | 0.67(0.55~0.78) | 72.90 | 71.10 | 76.10 | 67.50 | 73.26 |
| 胆囊壁不连续 | 0.60(0.48~0.72) | 45.50 | 32.30 | 54.30 | 25.00 | 59.30 |
| 宽基底 | 0.64(0.52~0.76) | 64.30 | 66.70 | 78.30 | 50.00 | 65.11 |
| 超声造影特征 | ||||||
| 动脉期高增强 | 0.59(0.42~0.76) | 56.20 | 61.50 | 89.10 | 20.00 | 56.98 |
| 静脉期早廓清 | 0.70(0.59~0.81) | 77.10 | 62.70 | 58.70 | 80.00 | 68.60 |
注:AUC为ROC曲线下面积;95%CI为95%置信区间 |
表3 超分辨超声各定量特征鉴别胆囊肿瘤性息肉与胆囊非肿瘤性息肉的诊断效能比较 |
| 诊断特征 | AUC(95%CI) | 敏感度(%) | 特异度(%) | 阳性预测值(%) | 阴性预测值(%) | 准确性(%) |
|---|---|---|---|---|---|---|
| 血流形态 | ||||||
| Ⅱ级及以上血流 | 0.82(0.73~0.92) | 83.00 | 82.10 | 84.80 | 80.00 | 82.56 |
| 定量参数 | ||||||
| 分形维数>1.55 | 0.77(0.66~0.87) | 77.10 | 76.30 | 80.40 | 72.50 | 76.74 |
| 血流速度>17.10(mm/s) | 0.75(0.66~0.86) | 84.00 | 50.00 | 67.70 | 50.00 | 72.09 |
| 血流容积>6.37 | 0.75(0.66~0.86) | 78.30 | 67.50 | 73.50 | 73.00 | 73.26 |
| 灌注指数>6.53 | 0.75(0.64~0.86) | 82.60 | 67.50 | 74.50 | 77.10 | 75.58 |
| 血管密度>30.78 | 0.71(0.59~0.82) | 87.00 | 60.00 | 71.40 | 80.00 | 74.42 |
| 方向方差>1745.36 | 0.55(0.43~0.68) | 57.80 | 59.10 | 67.50 | 32.50 | 58.13 |
| 速度方差>178.96 | 0.57(0.44~0.69) | 64.30 | 56.80 | 58.70 | 62.50 | 61.63 |
| 诊断标准1 | 0.84(0.75~0.93) | 74.60 | 92.60 | 95.70 | 62.50 | 80.23 |
| 诊断标准2 | 0.82(0.72~0.91) | 87.50 | 76.10 | 76.10 | 87.50 | 81.40 |
注:AUC为ROC曲线下面积;95%CI为95%置信区间;诊断标准1为满足血管形态Ⅱ级及以上、分形维数>1.55任一指标即诊断为肿瘤性息肉;诊断标准2为同时满足血管形态Ⅱ级及以上、分形维数>1.55两项即诊断为肿瘤性息肉 |
表4 超声单一或多模态参数鉴别胆囊肿瘤性息肉与非肿瘤性息肉的诊断效能比较 |
| 诊断模型 | AUC(95%CI) | 敏感度(%) | 特异度(%) | 阳性预测值(%) | 阴性预测值(%) | 准确性(%) |
|---|---|---|---|---|---|---|
| 模型1(常规超声) | 0.71(0.60~0.82) | 69.00 | 78.60 | 87.00 | 55.00 | 72.09 |
| 模型2(超声造影) | 0.70(0.59~0.81) | 77.10 | 62.70 | 58.70 | 80.00 | 68.60 |
| 模型3(超分辨超声) | 0.82(0.73~0.92) | 83.00 | 82.10 | 84.80 | 80.00 | 82.56 |
| 模型4(常规超声+超声造影) | 0.72(0.61~0.83) | 81.30 | 63.00 | 56.50 | 85.00 | 69.77 |
| 模型5(常规超声+超分辨超声) | 0.83(0.73~0.92) | 84.40 | 80.50 | 82.60 | 82.50 | 82.60 |
| 模型6(常规超声+超声造影+超分辨超声) | 0.84(0.79~0.95) | 83.00 | 82.10 | 84.80 | 80.00 | 82.60 |
注:AUC为ROC曲线下面积;95%CI为95%置信区间;常规超声标准为息肉最大径≥14.5 mm;超声造影标准为静脉期早廓清;超分辨超声标准为血流形态Ⅱ级及以上;单一及组合模型的AUC比较:模型3与模型1相比,P=0.001;模型3与模型2相比,P=0.008;模型5与模型4相比,P=0.077;模型6与模型4相比,P=0.048 |
五、超分辨超声血流形态分级的判读一致性分析
表5 不同医师评估超分辨超声下胆囊息肉样病变血流形态的一致性比较(例) |
| 医师1 | 医师2 | 总计 | Kappa值 | ||
|---|---|---|---|---|---|
| Ⅰ级血管模式 | Ⅱ级血管模式 | Ⅲ级血管模式 | |||
| Ⅰ级血管模式 | 34 | 3 | 1 | 38 | 0.78 |
| Ⅱ级血管模式 | 3 | 15 | 2 | 20 | |
| Ⅲ级血管模式 | 2 | 1 | 25 | 28 | |
| 总计 | 39 | 19 | 28 | 86 | |