

2023 , Vol. 20 >Issue 12: 1287 - 1293
DOI: https://doi.org/10.3877/cma.j.issn.1672-6448.2023.12.012
Sonazoid®超声造影不同参数成像效果的体外研究
Copy editor: 汪荣
收稿日期: 2023-04-30
网络出版日期: 2024-03-05
版权
In vitro study of different parameters of contrast-enhanced ultrasound with Sonazoid®
Received date: 2023-04-30
Online published: 2024-03-05
Copyright
探讨Sonazoid®超声造影(CEUS)在不同造影剂剂量浓度、机械指数(MI)和造影模式下的成像效果。
采用医用超声耦合剂和乳胶软管制备体外模型。Sonazoid®超声造影剂稀释混匀备用。在不同造影模式[振幅调制成像(Gen)和脉冲相位反转成像(Hres1)]下,每一剂量浓度组(0.1、0.15、0.2 ml/L)分别在9个MI值(0.16、0.19、0.22、0.25、0.27、0.33、0.4、0.5及0.7)条件下向乳胶软管内缓慢匀速推注Sonazoid® 24 ml。探头固定扫查切面为乳胶管最大长轴切面。应用时间-强度曲线定量分析不同剂量浓度、不同造影模式及不同MI条件下,管内造影剂的增强强度、衰减程度和微泡增强持续时间。
增强强度在0.15 ml/L组高于0.1 ml/L组[(31.0±5.0)dB vs(28.7±5.0)dB,P<0.001],而衰减程度差异无统计学意义[1.0(0.3,1.8)dB vs 0.6(0.2,1.4)dB,P=0.064]。Hres1的增强强度及衰减程度大于Gen模式[(33.4±5.4)dB vs(28.9±4.5)dB,P<0.001;1.0(0.4,2.1)dB vs 0.8(0.3,1.7)dB,P=0.027],与Gen模式相比,Hres1模式微泡增强持续时间更短[(6.9±1.8)s vs(7.5±2.5)s,P=0.003]。Hres1模式下MI=0.25及Gen模式下MI=0.22时可以较好平衡微泡增强持续时间和增强强度。
Sonazoid®-CEUS的临床应用需考虑造影剂剂量浓度、MI、造影模式等因素的影响,以达到理想的成像效果。
覃斯 , 刘一铭 , 周静雯 , 李昀芸 , 刘广健 . Sonazoid®超声造影不同参数成像效果的体外研究[J]. 中华医学超声杂志(电子版), 2023 , 20(12) : 1287 -1293 . DOI: 10.3877/cma.j.issn.1672-6448.2023.12.012
To investigate the influence of dose, mechanical index (MI), and imaging techniques on contrast-enhanced ultrasound (CEUS) with Sonazoid®.
In vitro models were prepared utilizing medical ultrasonic couplants and latex hoses. Sonazoid® was diluted and prepared. In each dose group (0.1 ml/L, 0.15 ml/L, and 0.2 ml/L), Sonazoid® (24 ml) was injected slowly and uniformly into the tube at 9 MI values (0.16, 0.19, 0.22, 0.25, 0.27, 0.33, 0.4, 0.5, and 0.7) using different imaging techniques [power modulation imaging (Gen) and pulse inversion imaging (Hres1)]. The probe was fixed to the maximum long-axis section of the latex hose for scanning. Quantitative analysis was performed using time-intensity curves to assess the enhancement, attenuation, and sustained enhancement time of microbubbles in the tube under different doses, MI values, and imaging techniques.
The enhancement in the 0.15 ml/Lgroup was higher than that of the 0.1 ml/L group [(31.0±5.0) dB vs (28.7±5.0) dB, P<0.001], but there was no significant difference in attenuation between them [1.0 (0.3, 1.8) dB vs 0.6 (0.2, 1.4) dB, P=0.064]. The enhancement and attenuation of Hres1 were higher than those of Gen [(33.4±5.4) dB vs (28.9±4.5) dB, P<0.001; 1.0 (0.4, 2.1) dB vs 0.8(0.3, 1.7) dB, P=0.027], and the sustained enhancement time of microbubbles was shorter [(6.9±1.8) s vs (7.5±2.5) s, P=0.003]. The balance between the enhancement and sustained enhancement time of microbubbles was obtained at MI=0.25 in Hres1 and MI=0.22 in Gen, respectively.
The clinical application of CEUS with Sonazoid® should consider the influence of dose, MI, and imaging technique, in order to achieve ideal imaging effects.
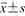 表示;ΔI外为不满足正态分布的计量资料,以M(P25,P75)表示。按剂量浓度(0.1、0.15、0.2 ml/L)分组,ΔI内、ΔT的组间比较先采用随机区组设计方差分析进行总体比较,再采用配对t检验进行两两比较;ΔI外的组间比较先采用Friedman的统计检验进行总体比较,再采用配对Wilcoxon符号秩检验进行两两比较,以P<0.017为差异有统计学意义。按造影模式(Gen和Hres1)分组,ΔI内、ΔT的组间比较采用配对t检验,ΔI外的组间比较采用配对Wilcoxon符号秩检验,以P<0.05为差异有统计学意义。计算Pearson相关系数分析微泡增强持续时间与MI的相关性:>0.8~1.0为极强相关,>0.6~0.8为强相关,>0.4~0.6为中等程度相关,>0.2~0.4为弱相关,≤0.2为极弱相关或无相关。按不同MI值分组,相同造影模式下ΔI内的组间比较先采用方差分析进行总体比较,再采用Games-Howell检验进行两两比较,以P<0.05为差异有统计学意义。
表示;ΔI外为不满足正态分布的计量资料,以M(P25,P75)表示。按剂量浓度(0.1、0.15、0.2 ml/L)分组,ΔI内、ΔT的组间比较先采用随机区组设计方差分析进行总体比较,再采用配对t检验进行两两比较;ΔI外的组间比较先采用Friedman的统计检验进行总体比较,再采用配对Wilcoxon符号秩检验进行两两比较,以P<0.017为差异有统计学意义。按造影模式(Gen和Hres1)分组,ΔI内、ΔT的组间比较采用配对t检验,ΔI外的组间比较采用配对Wilcoxon符号秩检验,以P<0.05为差异有统计学意义。计算Pearson相关系数分析微泡增强持续时间与MI的相关性:>0.8~1.0为极强相关,>0.6~0.8为强相关,>0.4~0.6为中等程度相关,>0.2~0.4为弱相关,≤0.2为极弱相关或无相关。按不同MI值分组,相同造影模式下ΔI内的组间比较先采用方差分析进行总体比较,再采用Games-Howell检验进行两两比较,以P<0.05为差异有统计学意义。表1 脉冲相位反转成像(Hres1模式)和振幅调制成像(Gen模式)不同机械指数下的增强强度变化( |
| 造影模式 | MI=0.16 | MI=0.19 | MI=0.22 | MI=0.25 | MI=0.27 | MI=0.33 | MI=0.4 | MI=0.5 | MI=0.7 | F值 | P值 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Hres1模式 | 29.8±4.5a | 32.5±2.6a | 32.5±4.6a | 35.8±3.4 | 33.9±3.8 | 34.7±4.0 | 34.9±4.5 | 34.4±4.6 | 31.7±9.2 | 4.9 | <0.001 |
| Gen模式 | 25.5±4.0b | 27.3±3.6b | 28.0±5.1 | 27.6±4.3 | 28.9±5.1 | 30.8±4.4 | 30.0±4.1 | 30.0±4.7 | 27.0±6.9 | 4.2 | <0.001 |
注:Gen为振幅调制成像;Hres1为脉冲相位反转成像;MI为机械指数;Hres1模式下,与MI=0.25相比,aP<0.05;Gen模式下,与MI=0.33相比,bP<0.05(方差齐性检验P=0.006,两两比较采用Games-Howell检验) |
| 1 |
|
| 2 |
|
| 3 |
陈彦玲, 王文平. 超声造影在肝细胞性肝癌诊疗中的应用进展[J]. 中华超声影像学杂志, 2020, 10(29): 916-920.
|
| 4 |
|
| 5 |
|
| 6 |
陈烁淳, 许敏, 顾炯辉, 等. 超声造影剂Sonazoid的研究进展[J]. 中华超声影像学杂志, 2020, 29(7): 636-641.
|
| 7 |
王艳红, 钱林学. 造影剂剂量浓度对健康成年人肝脏超声造影定量分析的影响[J/CD]. 中华医学超声杂志(电子版), 2014, 11(12): 953-957.
|
| 8 |
顾炯辉, 何蒙娜, 许敏, 等. 基于时间-强度曲线评价SonoVue和Sonazoid在肝癌中的价值[J].中国超声医学杂志, 2020, 36(12): 1133-1136.
|
| 9 |
位红芹, 付伸伸, 马穗红, 等. 不同机械指数超声对微泡的作用[J]. 中国医学影像技术, 2021, 37(5): 648-651.
|
| 10 |
|
| 11 |
|
| 12 |
张程, 李昶田, 李俊来. 诊断超声的生物效应与安全性研究进展[J]. 中国医学装备, 2021,18(3):172-176.
|
/
| 〈 |
|
〉 |